Cum pentru a determina tipul de grilaj de cristal
Așa cum poate fi ușor de ghicit din denumirea unui tip grilaj metalic are loc în metale. Aceste substanțe sunt caracterizate, temperatura de topire ridicată în mod tipic, luciu metalic, duritate, sunt bune conductoare de electricitate. Nu uitați că sunt atomi sau ioni neutri sau incarcati pozitiv la nodurile Grile de acest tip. Intre nodurile - electroni și migrația, care asigură o conductivitate electrică ridicată a unor astfel de materiale.
tip Ionic rețea cristalină. Rețineți că este inerent în oxizi și săruri. Un exemplu tipic - toate cristalele cunoscute de sare, clorură de sodiu. Nodurile laticile sunt alternate alternativ pozitiv și încărcat negativ ioni. Astfel de materiale sunt în general refractare volatilitate, scăzută. După cum puteți ghici, ei au tipul de ioni legăturii chimice.
Atomic rețea cristalină de tip substanțe simple, inerente - nemetale, care, în condiții normale, reprezintă corpuri solide. De exemplu, sulf, fosfor, carbon. Nodurile acestor latici sunt atomi neutri, legați unul de celălalt printr-o legătură chimică covalentă. Aceste substanțe refractaritate inerente, insolubilitate în apă. Unele (de exemplu, carbon sub formă de diamant) - extrem de mare duritate.
În cele din urmă, ultimul tip de grilaj - moleculare. Aceasta apare la substanțe, care sunt, în condiții normale într-o formă lichidă sau gazoasă. Cum, din nou, poate fi ușor de înțeles din titlu, nodurile laticile - molecula. Acestea pot fi fie specii non-polare formă (simplu gaz Cl2 y tip, O2) și polare (exemplul cel mai cunoscut - H2O Water). Substanțele care au un astfel de tip zăbrele nu conduc curent, volatile, au puncte de topire scăzute.
Astfel, pentru a determina cu certitudine ce tip grilaj este o substanță, ar trebui să înțeleagă ce clasă de substanțe se aplică ceea ce are proprietăți fizico-chimice.
In cristale de specii chimice (molecule, atomi și ioni) sunt dispuse într-o anumită ordine, în anumite condiții, ele formează poliedre regulate simetrice. Există patru tipuri de cristal - Grile ionice, atomice, moleculare și metal.

Starea cristalină se caracterizează prin ordine cu rază lungă în aranjamentul particulelor, precum simetria rețelei cristaline. Cristalele solide se numesc formarea tridimensionale, în care aceeași structură elementul se repetă în toate direcțiile.
Forma corectă a cristalelor datorită structurii lor interne. În cazul în care înlocuiesc moleculele, atomii și punctele de ioni în loc de centrele de greutate ale acestor particule, veți obține o distribuție regulată tridimensională - rețeaua cristalină. elemente care se repetă de structura sa numite celule elementare, si puncte - noduri zăbrele. Există mai multe tipuri de cristale, în funcție de particulele pe care le constituie, precum și natura legăturii chimice dintre ele.
Grile ionice
Cristale ionice formează anioni și cationi, între care există o legătură ionică. Prin acest tip de cristale sunt săruri și hidroxizi de cele mai multe metale. Fiecare cation r anion este atras și respins de ceilalți cationi, deci într-un cristal ionic este imposibil să se izoleze molecule unice. Crystal poate fi văzută ca o moleculă uriașă, iar dimensiunea acesteia nu este limitat, acesta este capabil de a adăuga ioni noi.
Atomic rețeaua cristalină
atomii individuali sunt combinate prin legături covalente în cristale atomice. Sub formă de cristale ionice, ele pot fi, de asemenea, văzută ca o moleculă uriașă. În acest caz, cristalele atomice sunt foarte solide și durabile, sunt conductoare slabe de energie electrică și termică. Ele sunt practic insolubile, acestea sunt caracterizate prin reactivitate scăzută. Substanțele cu zăbrele atomice se topesc la temperaturi foarte ridicate.
cristale moleculare
zăbrele cristalin molecular format din molecule ale căror atomi sunt legături covalente combinate. Din acest motiv, moleculele sunt forțe moleculare slabe. Aceste cristale sunt diferite duritate scăzută, cu punct de topire scăzut și fluiditate ridicată. Substanțele pe care le formează, și se topește și soluțiile lor nu conduc curentul electric.
Grile metalice
Rețelele cristaline ale atomilor metalici sunt aranjate la densitatea maximă, acestea sunt conexiunea delocalizat, ele sunt distribuite pe întreaga cristal. Aceste cristale sunt opace, caracterizate printr-un luciu metalic, ușor deformat, astfel bune conductoare de energie electrică și termică.
Această clasificare descrie doar cazurile limitative, majoritatea cristalelor de substanțe anorganice aparțin tipurilor intermediare. - Molecular-covalent, covalentă, ionică, etc. Ca un exemplu de cristal de grafit, în interiorul fiecărui strat avea legături covalent-metalice, dar intre straturi - moleculare.
Diamond - este un mineral aparținând unei modificări alotropice carbon. O trăsătură distinctivă este duritate ridicată, care este pe bună dreptate, îi dă titlul de solide. Diamond este un mineral rar, dar în același timp și cea mai răspândită. duritate excepțională își găsește aplicarea sa în inginerie mecanică și industrie.

Diamond are un grilaj atomic. Atomii de carbon care constituie moleculele de cadru sunt aranjate într-un tetraedru, astfel încât diamantul are o rezistență ridicată. Toți atomii sunt legați prin legături covalente puternice, care se formează pe baza structurii electronice a moleculei.

atom de carbon este sp3 hibridizare a orbitali, care sunt dispuse la un unghi de 109 de grade și 28 de minute. orbitali hibride suprapunere are loc într-o linie dreaptă în plan orizontal.
Astfel, atunci când suprapunerea orbitali este format la un unghi centrat tetraedru, care face parte din sistemul cubic, astfel încât se poate spune că diamantul are o structură cubică. Această structură este considerată una dintre cele mai durabile în natură. Toate tetraedre formează straturi de o rețea tridimensională de inele atomi hexaatomice. O astfel de rețea stabilă de legături covalente și distribuția tridimensională conduce la o rezistență suplimentară cu zăbrele.
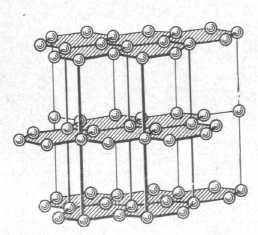
Rețeaua cristalină a diamant este destul de complicată. Se compune din două sublattices simple. Regiunea spațiului situată mai aproape de un anumit atom decât alți atomi la zăbrele diamant este triakisov tetraedru trunchiat. Acest tip de grilaj posedă, de asemenea, siliciu, germaniu și staniu, de preferință alfa-formă.
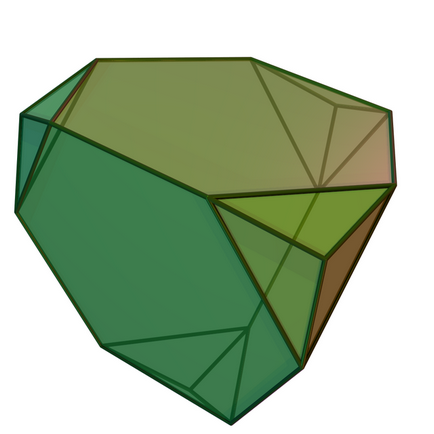
Triakisov tetraedru trunchiată este un poliedru alcătuit din patru hexagoane și douăsprezece triunghiuri isoscele. Acesta poate fi folosit pentru tessellation spațiu tridimensional. Ca un exemplu de tessellation poate fi considerat un pătrat care trebuie tăiate pe diagonală, adică pătrat în forma un mozaic două triunghiuri. Tessellation se îmbunătățește realismul modelului tridimensional, aplicat la rețeaua cristalină a diamantului face mai realist.
În momentul de față, știința a ajuns la producția de diamante sintetic. Pentru sunt folosite sinteza acestor cristale, în mod tipic ridicat de carbon din aliaj de mangan-nichel sau plasmă de înaltă frecvență, concentrată pe un substrat, în care este format diamantul în sine. La producerea unui mineral în acest mod, rețelelor cristaline diferite de zăbrele, care are un diamant natural. Schimbarea straturilor de carbon, în legătură cu care acestea sunt plasate la întâmplare. De aceea, cristalele obținute în acest mod au o rezistență mai mică și o friabilitate suficient de mare.
