Numerele cuantice ale electronilor
numere cuantice - parametri de energie care determină starea unui electron și un tip de orbital atomic în care se află.
numere cuantice - parametri de energie care determină starea unui electron și un tip de orbital atomic în care se află.
1. Principalul Chislon cuantică caracterizează energia totală a electronului și mărimea orbital. Este nevoie de o valoare întreagă de 1: n = 1, 2, 3, 4, 5, 6, 7.
2. Orbital (lateral) cuantice chislol caracterizează forma orbitali atomice și ia valori de la 0 la n-1. 0, 1, 2, 3, ..., n-1.
- Cu orbital număr cuantic l = 0 se numesc orbitali S-;
- Cu orbital număr cuantic l = 1 se numesc orbitali P- (tipul 3);
- Numărul cuantic orbital l = 2 se numește orbitali d- (5 tipuri);
- Cu numarul cuantic orbital l = 3 se numește orbitali F- (7 tipuri);
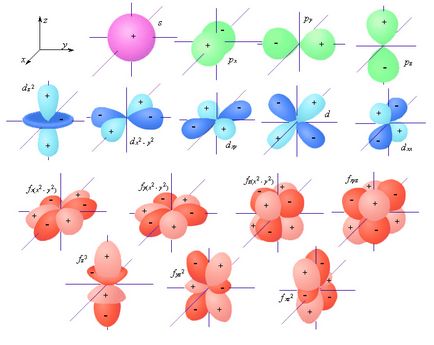
Electronice, care posedă proprietățile particulei și a valurilor se mișcă în jurul miezului pentru a forma un nor de electroni, forma care, în S-, P-, d-, f-, g -states diferite.
Dacă l = 0 (S-orbital) norul de electroni este sferic și nu sa orientat în spațiu.
Dacă l = 1 (orbital P-) norul de electroni are forma unei halteră.
orbitali d- și F- au o formă mai complexă.
3. Numărul cuantic magnetic al chislom orbital caracterizează aceeași formă și orientarea relativă a acestora la un câmp electric sau magnetic extern. Numărul cuantic m este un număr întreg în intervalul -l, ... -1, 0, +1, ... + l. Pentru fiecare valoare a permis 2l + 1 valori de numărul m. De exemplu, dacă l = 1. atunci m este 2 x 1 + 1. și anume Trei valori: -1, 0, +1.
4. chislos cuantice spin caracterizează rotația electronilor în jurul axei sale și durează doar două valori: +1/2 (↑) și -1/2 (↓).