Covalente legături chimice - este
definiție
Legătură covalentă se numește o legătură chimică este formată datorită socializării atomilor lor de electroni de valență. O condiție este formarea unei legături covalente suprapunere a orbital atomic (AO), care sunt aranjate electroni de valență. In cel mai simplu caz, două suprapuse AB duce la formarea a două moleculare orbitale (MO), care leagă MO și antibonding (antibonding) MO. împerecheat electroni dispuse la un OM energetic obligatoriu inferior:
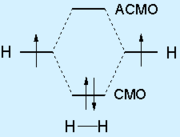
lipirea
Legătură covalentă (legătură atomică, legătură covalentă) - legătură între doi atomi de socializare datorită (partajare de electroni) doi electroni - unul din fiecare atom:
Din acest motiv, legătură covalentă este direcțională. O pereche de electroni în comunicare aparține simultan atât atomii de legătură, de exemplu:
Tipuri de legătură covalentă
Există trei tipuri de legătură chimică covalentă, altele decât mecanismul de formare a acesteia:
1. o singură legătură covalentă. Pentru formarea sa fiecare atom furnizează un electron nepereche. În formarea unei singure legături covalente invinuite ale atomilor rămân neschimbate. În cazul în care atomii care formează aceeași legătură unică covalentă, atunci adevăratele acuzații ale atomilor în moleculă sunt de asemenea identice, deoarece atomii formează o legătură pereche la fel de competenți electroni socializat, o astfel de conexiune este numită o legătură covalentă nepolară. Dacă atomii sunt diferite, atunci rata de proprietate pereche socializați de electroni este determinat de diferența în electronegativities de atomi, atomul cu electronegativitatea mai mare măsură mai mare are o pereche de electroni, și, prin urmare, o sarcină adevărată este negativă, atomul cu electronegativitate mai mică dobândește, respectiv, aceeași sarcină magnitudine dar cu un semn pozitiv.
2. Legăturile donor-acceptor. Pentru formarea acestui tip de o legătură covalentă, ambii electroni are unul dintre atomii (donor), al doilea dintre atomii implicate în formarea legăturii se numește un acceptor. Molecula rezultată este sarcina formală a atomului donor este incrementat, iar încărcătura formală a atomului acceptor decrementat.
3. semipolară legătura. Acest tip de o legătură covalentă se formează între un atom având o pereche de electroni unshared (azot. Fosfor. Sulf. Halogeni și m. P.) și atomul cu doi electroni nepereche (oxigen. Sulf). formarea legăturii semi-polar are loc în două etape:
1. Oxidarea (transferul unui electron) atom cu atom NEP cu doi electroni nepereche. Ca rezultat, atomul cu NEP convertit la cation radicalul (încărcat pozitiv de particule cu un electron nepereche) și atomul cu doi electroni nepereche - un anion radical (particule încărcate negativ cu un electron nepereche).
2. socializarea electroni nepereche (ca în cazul unei legături covalente simplă).
În formarea unui atom cu o legătură semipolar NEP crește sarcina sa formală pe unitate, iar atomul cu doi electroni nepereche reduce sarcina lor formală pe unitate. mecanisme de unire Flash-clipuri chimice pot fi vizualizate aici
Sigma (σ) -, pi (π) -bond - o descriere aproximativă a tipurilor de legături covalente în molecule organice, σ-bond este caracterizat prin aceea că densitatea norului de electroni este maximă de-a lungul axei care unește nucleele atomilor. In formarea π -bond efectuat așa-numita suprapunere laterală a norilor de electroni, iar densitatea norului de electroni este maximal „mai sus“ și „jos“, planul σ-legătura. De exemplu, luați etilena. acetilenă și benzen.
Etilen molecula C2 H4 are o legătură dublă CH2 = CH2. formula electronică: H: C :: C: H. Miezuri de atomi de etilenă sunt coplanare. Trei nori de electroni din fiecare atom de carbon care formează trei legături covalente la alți atomi în același plan (cu unghiul dintre ele aproximativ 120 °). Cloud atom de carbon al patrulea al unui electron de valență situate deasupra și dedesubtul planului moleculei. Astfel de nori de electroni ambii atomi de carbon se suprapun parțial deasupra și sub planul moleculei, formează o a doua legătură între atomii de carbon. În primul rând, o legătură covalentă puternică între atomii de carbon se numește σ-legătură; în al doilea rând, mai puțin puternică legătură covalentă se numește π-obligațiuni.
Molecula liniară de acetilenă
Este sigma legături între atomii de carbon și hidrogen, un σ-legătură între doi atomi de carbon și doi π -bond între atomii de carbon. Două π -bond situate deasupra domeniului de aplicare al sigma obligațiuni în două planuri reciproc perpendiculare.
Toti cei sase atomi de carbon, benzen moleculă ciclică C6 H6 într-un singur plan minciună. Între atomii de carbon din planul inelului sunt σ-legătură; aceeași comunicare sunt la fiecare atom de carbon cu atomi de hidrogen. În implementarea acestor conexiuni atomi de carbon petrece trei electroni. Norii patra electroni de valență ale atomilor de carbon având optari formă situate perpendicular pe planul moleculei de benzen. Fiecare astfel de nor se suprapune cu norii de electroni aceiași atomi de carbon adiacenți. Molecula de benzen nu sunt formate trei -bond π separat și un singur π este sistemul de electroni al celor șase electroni comune tuturor atomilor de carbon. Legătură între atomii de carbon din molecula de benzen complet identice.
Legăturii covalente formate prin schimbul de electroni (pentru a forma o pereche de electroni comune), care apar în timpul suprapunerii de nori de electroni. În formarea unei legături covalente implicând norii de electroni ai celor doi atomi. Există două tipuri principale de legătură covalentă:
- Legătura covalentă se formează între atomii metaloid nepolare din același element chimic. Aceste comunicări sunt substanțe simple. de exemplu, O2; N2; C12.
- legătură covalentă polară se formează între atomii de diferite nemetalelor.
În cazul, de exemplu, cu HCI. densitatea totală a electronilor este deplasată spre partea de clor, în care un atom de clor are loc o sarcină negativă parțială. un atom de hidrogen - un rezultat pozitiv parțial.
Exemple de substanțe cu o legătură covalentă
O simplă legătură covalentă atomii legat în moleculele de gaz simplu (H2. Cl2 și colab.) Și compușii (H2O, NH3. CH4. CO2. HCl și colab.). Compușii cu o legătură donor-acceptor - cation de amoniu NH4 +. tetrafluorborat anion BF4 - și alți compuși cu o legătură semipolar -. protoxidul de azot N2 O, O - -PCl3 +.
Cristale covalente izolatori sau semiconductori. Exemple tipice de cristale atomice (atomii care sunt interconectate prin legături covalente (atomice)) poate servi ca un diamant. germaniu și siliciu.
Vezi ce o „legătură chimică covalentă“ în alte dicționare:
COMMUNICATIONS CHIMICE - legătura dintre atomii din moleculă sau Moi. compus care rezultă din transferul sau e-mail, de la un atom la altul, o nouă pereche e socializare (sau grup) atomi. Forțele care conduc la X. cu. Coulomb, dar X. cu. descrise în ceea ce privește ... enciclopedie fizică
COMMUNICATIONS CHEMICAL - atomi de interacțiune, în care electronii aparținând doi atomi diferiți (grupuri) sunt comune (socializată) pentru cei doi atomi (grupuri), provocând cuplarea lor la molecule si cristale. Există două tipuri de bază de X. c. ion ... ... Cele mai multe Polytechnique Encyclopedia
CHIMICE COMMUNICATIONS - CHEMICAL COMMUNICATIONS, mecanismul prin care atomii sunt unite pentru a forma o moleculă. Există mai multe tipuri de astfel de conexiune, fie bazată pe atragerea de sarcini opuse, sau pe formarea de configurații stabile prin schimbul de electroni. ... ... enciclopedie științifică și tehnică
Legătura chimică - legătură, interacțiunea atomilor care face ca moleculele lor compuse și cristale. Operarea cu forțe legături chimice sunt în principal de natură electrică. formarea legăturii chimice este însoțită de o restructurare a ... ... Illustrated Dicționarul Enciclopedic
Legătura chimică - atomi de atracție reciprocă, ceea ce duce la formarea moleculelor și cristalelor. Noi spunem că o moleculă sau cristal există între atomii adiacenți H. p. Valența atomului (ce detaliu mai jos) arată numărul de link-uri ... Marea Enciclopedie Sovietică
legătură chimică - [legătură chimică (legare)] mutuale atomi de atracție, ceea ce duce la formarea moleculelor și cristalelor. Valența atomului indică numărul de legături formate cu atomul de date adiacente. Termenul „structură chimică“ a fost introdus Academician A. M. Butlerov în ... ... Dicționarul Enciclopedic metalurgie
Liantul chimică ionic - Ionic legătură puternică legătura chimică formată între atomii cu o diferență mare electronegativitate, la care perechea de electroni totală este complet transferat la atomul cu o mai mare electronegativitate. Un exemplu este un compus de CsF ... Wikipedia
Comunicații chimice - interacțiune Legătura chimică atomi fenomen cauzat prin suprapunerea de nori de electroni particule de legare este însoțită de reducerea energiei totale a sistemului. Termenul „structură chimică“ a fost introdus pentru prima dată A. M. Butlerov în 1861 ... ... Wikipedia
Comunicare (chimie) - interacțiune Legătura chimică atomi fenomen cauzat prin suprapunerea de nori de electroni particule de legare este însoțită de reducerea energiei totale a sistemului. Termenul „structură chimică“ a fost introdus pentru prima dată A. M. Butlerov în 1861 ... ... Wikipedia